干货满满!深圳二类医疗器械经营备案条件大盘点
作者:小奥 | 发布时间:2025-06-11
一、办理资质要求
1. 主体资格
需以公司为主体申请,个体工商户不可办理。
2. 人员配备
配备医疗器械相关技术人员及质量管理人员(如工程师、质检员)。
法人兼任企业负责人需大专以上学历(专业不限);质量负责人需大专以上学历、相关专业(如医疗器械、生物医学工程等),且有3年以上工作经验。
3. 场地要求
经营场所面积≥60㎡(需提供房产证或租赁合同),划分办公、展示功能区。
仓储场地需满足温湿度控制等存储标准(可委托第三方仓储)。
二、必备申请材料
1. 基础文件
营业执照正副本、公章;
法定代表人身份证原件照片及联系电话;
大专以上学历证明(无专业限制)。
2. 场地证明
经营场所地理位置图、平面图;
产权证明或商品房买卖合同复印件(面积需标注)。
3. 管理文件
组织架构图;
经营设施/设备清单、医疗器械管理制度及工作流程目录。
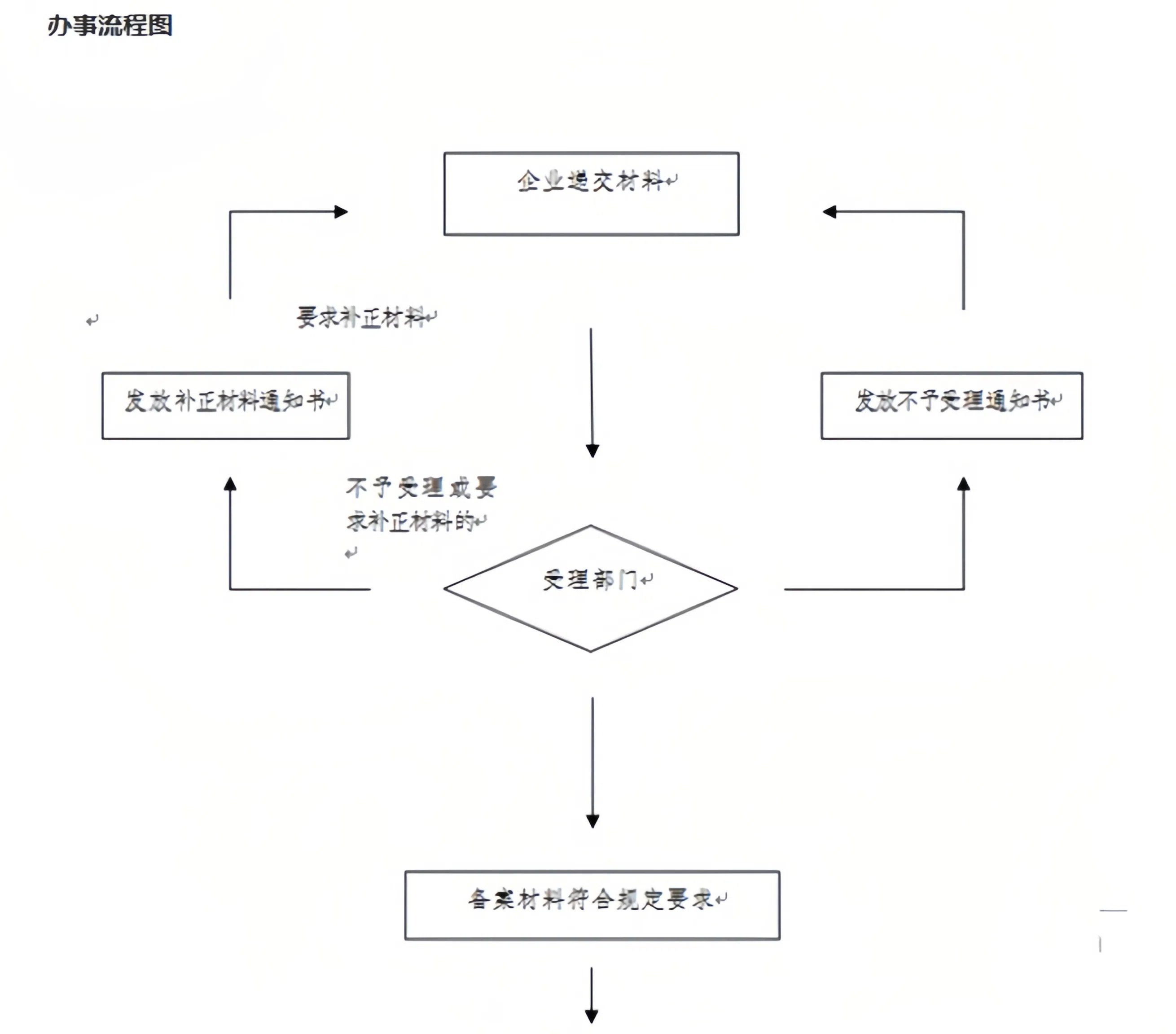
三、办理流程详解
1. 筹备阶段
确认技术人员资质(如学历证书、培训证明),质量负责人需完成备案。
确保经营场所与仓储条件符合《医疗器械经营质量管理规范》。
2. 申报阶段
线上渠道
登录深圳市药监局指定备案系统,填写企业信息并上传材料电子版。
线下渠道
前往区行政服务大厅综合窗口提交纸质材料,现场咨询补正要求。
3. 审核与发证
材料初审:部门当场核验材料,缺漏项一次性告知补正;材料合格即受理。
审批制证:审核通过后当场办结,企业自行登录系统下载打印《二类医疗器械经营备案凭证》。
监管后置:备案后监管部门可能按规范进行现场核查(非必查,特殊情况抽查)。
深圳二类医疗器械备案流程清晰,核心在于人员资质合规、场地达标及材料齐全,如需了解详情,欢迎咨询小奥。








